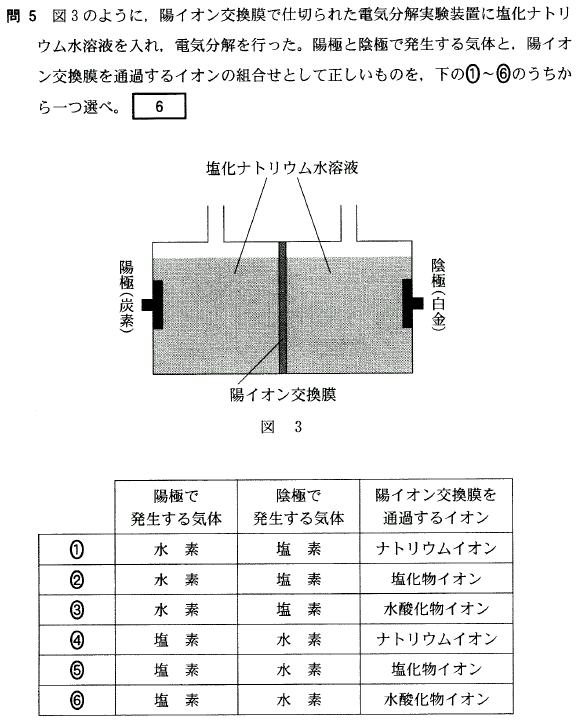
[6]正解④
左右それぞれの電気分解曹では、 NaCl → Na
+ + Cl
- のように電離していて、
これら Na
+ 、Cl
- が電極に引き付けられます。
陽極(+極)には、 Cl
- が引き付けられ、2Cl
- → Cl
2↑+ 2e
- で、塩素が発生します。
陰極(-極)には、Na
+ が引き付けられますが、Na
+ はイオン化傾向が大きいため電子を受け取らず、代わりにH
2Oが電子を受け取り、2H
2O + 2e
- → H
2↑+ 2OH
- で、水素が発生します。
さて、陽極では、Cl
- と Na
+ が同数存在して電荷が釣り合っていたのですが、Cl
- が減ったので、「Na
+ が余っている状態」と考えて下さい。
同様に、陽極では、Cl
- と Na
+ が同数存在して電荷が釣り合っていたのですが、OH
- が増えたので、負電荷 が余っている状態つまり「正電荷 が足りない状態」と考えて下さい。
これら、陰極の「Na
+ が余っている状態」、陽極の「正電荷 が足りない状態」は、「陽極から陰極に、陽イオン交換膜を経て Na
+ が移動する」ことで解消される、と考えて下さい。(陰極から陽極に、陰イオンが移動してもこの状態を解消できますが、陽イオン交換膜は陽イオンしか通せないので、陽イオンが移動する訳です)


